Gesynta Pharmas läkemedelskandidater utnyttjar en unik verkningsmekanism för att reducera inflammation och minska smärta. Genom att rikta in sig på mPGES-1, ett nyckelenzym i lokala inflammationer, har våra läkemedelskandidater förmågan att dämpa inflammatoriska processer med en betydligt högre precision än dagens tillgängliga läkemedel. Läs mer om våra läkemedelskandidater och hur de fungerar nedan.

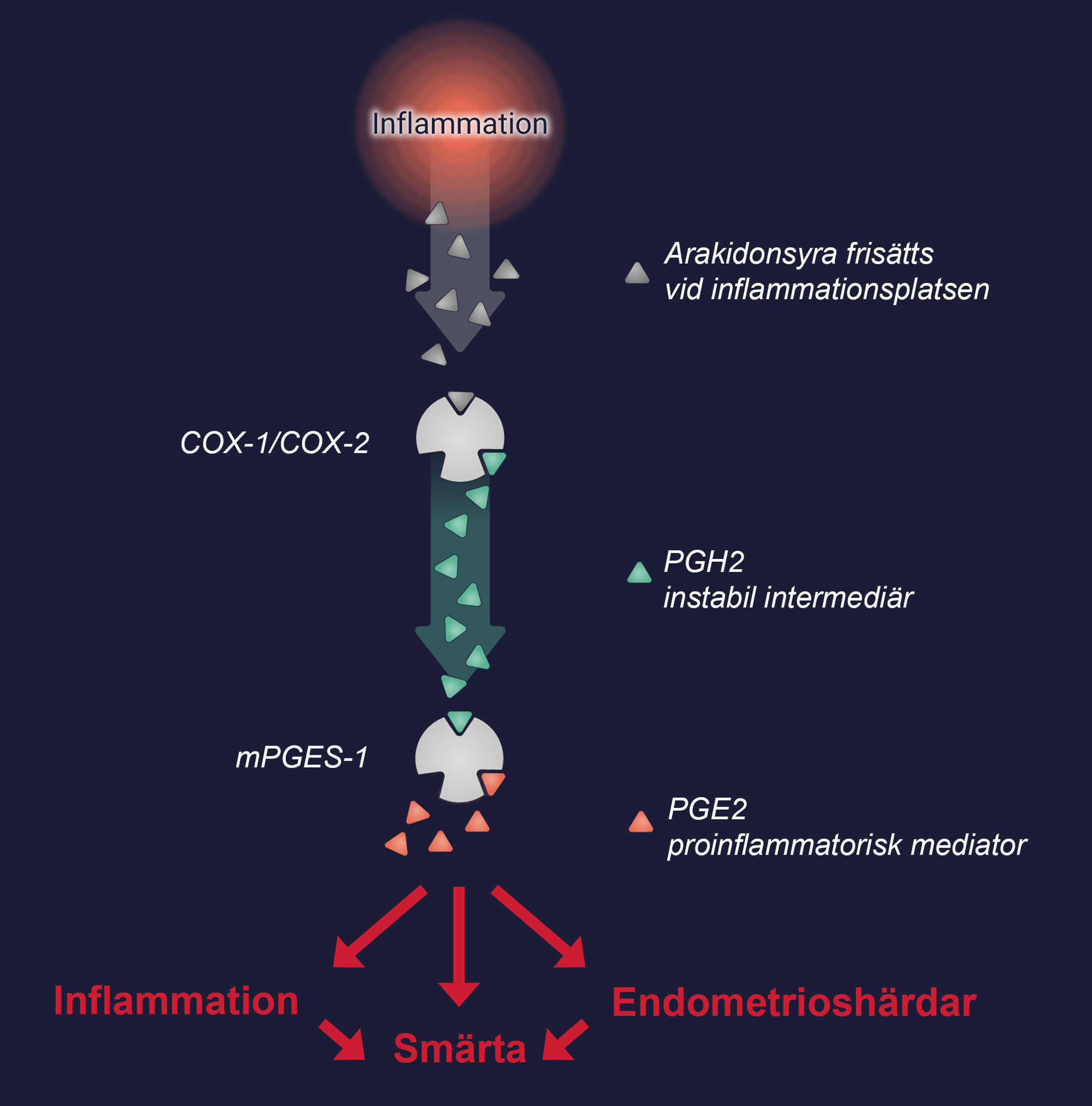
Gesynta Pharmas utvecklar läkemedelskandidater med en unik förmåga att selektivt hämma mikrosomalt prostaglandin E-syntas (mPGES-1), ett enzym som katalyserar bildning av inflammationsdrivande prostaglandin E2 (PGE2). Genom att hämma mPGES-1 minskar nivåerna av PGE2 vilket leder till antiinflammatoriska och smärtlindrande effekter.
Läs mer om vipoglanstat, i klinisk fas 2 för behandling av endometrios
Läs mer om GS-073 för behandling av kronisk inflammatorisk smärta